Metaller, Dayanıklı Azot-Azot Bağlarını Zayıflatmak için Nasıl İşbirliği Yapıyorlar

Fotoğraf-1: MIT kimyagerleri, gaz halindeki dinitrojenin, yani N2‘nin, bir demir-kükürt kümesine bağlandığında oluşan kompleksin yapısını belirlediler ve mikroorganizmaların (sarı renkte) azot-azot bağını (pembe ve yeşil) kırmak için nitrojenaz enzimini nasıl kullandıklarına dair ipuçları sundular. (1)
Tüm canlı hücreler için temel bir element olan azot, Dünya atmosferinin yaklaşık yüzde 78’ini oluşturur. Ancak çoğu organizma, amonyağa dönüşmedikçe, bu inert azottan yararlanamaz. İnsanoğlu endüstriyel amonyak sentezini icat edene kadar, gezegendeki hemen hemen tüm amonyak, atmosferde bulunan moleküler azotun üçlü bağını kırabilen tek enzime, “nitrojenazlara” sahip olan mikroorganizmalar tarafından üretildi.
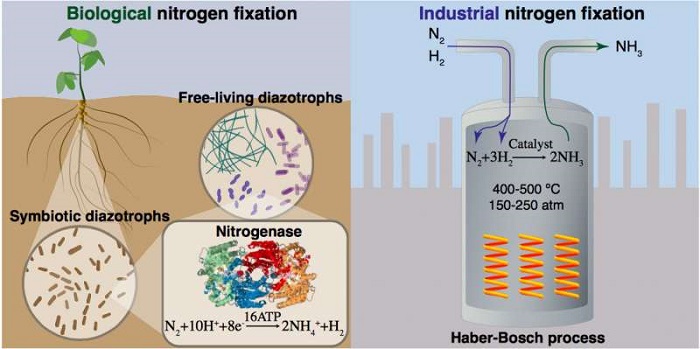
Fotoğraf-2: Azot bağlanması, doğal olarak nitrojenaz enzimi içeren bakteriler tarafından gerçekleştirilir. Endüstriyel işlem yoluyla ise demir bazlı katalizörlere ve doğal gazdan elde edilen büyük miktarlarda hidrojene dayanan yüksek sıcaklık ve yüksek basınçlı bir yapay prosesle, Haber-Bosch prosesi ile, gerçekleştirilebilir. (2)
Bu enzimler, bu kritik reaksiyonu gerçekleştirmeye yardımcı olan metal ve kükürt atomlarından oluşan kümeler içerir, ancak azot bağlanma mekanizması bugüne kadar tam olarak anlaşılamamıştır. İlk kez, MIT kimyagerleri N2‘ nin bu kümelere bağlanmasıyla oluşan bir kompleksin yapısını belirlediler ve bu kümelerin çok kararlı olan azot-azot bağını şaşırtıcı derecede zayıflatabildiğini keşfettiler.
MIT’de Kariyer Geliştirme Bölümü Kimya Yardımcı Doçenti ve çalışmanın kıdemli yazarı Daniel Suess, “Bu çalışma, kırılması zor olan, bu çok güçlü bir bağa sahip, gerçekten atıl olan molekülü aktive etmemizi sağlayan mekanizma hakkında fikir edinmemizi sağlıyor” diyor.
Şu anda Tulane Üniversitesi’nde yardımcı doçent olan eski bir MIT doktora sonrası öğrencisi olan Alex McSkimming, bugün Nature Chemistry‘de yayınlanan makalenin baş yazarıdır. (3)
Azot Fiksasyonu (Azot Bağlanması)
Azot, proteinlerin, DNA’nın ve diğer biyolojik moleküllerin kritik bir bileşenidir. Atmosferden azotu ayırmak için, ilk mikroorganizmalar, “azot bağlanması” adı verilen bir süreçle atmosferdeki serbest azot gazını (N2), toprakta sabit azota, yani amonyağa (NH3) dönüştüren nitrojenazlar ürettiler. Hücreler daha sonra bu amonyağı daha karmaşık azot içeren bileşikler oluşturmak için kullanabilirler.
Suess, “Büyük ölçeklerde sabit azota erişim yeteneği, yaşamın çoğalmasını sağlamada etkili oldu” diyor. “N2 gerçekten güçlü bir bağa sahip ve gerçekten kimyasal tepkimeye girmiyor, bu yüzden kimyacılar temelde onu inert bir molekül olarak nitelendirmişlerdir. Bu, yaşamın çözmesi gereken bir bulmaca: bu atıl molekül, yararlı kimyasal türlere nasıl dönüştürülüyor.”
Tüm nitrojenazlar bir dizi demir ve kükürt atomu içerir ve bazıları ayrıca molibden içerir. Dinitrojenin, amonyağa dönüşümü başlatmak için, bu kümelere bağlandığına inanılmaktadır. Bununla birlikte, bu etkileşimin doğası belirsizdir ve şimdiye kadar bilim insanları, N2’ nin bir demir-kükürt kümesine bağlanma mekanizmasını tanımlayamamışlardır.
Kimyagerler nitrojenazların N2‘yi nasıl bağladığını aydınlatabilmek için, doğal olarak oluşan kümeleri modellemede kullanabilecekleri daha basit demir-kükürt kümeleri tasarladılar. En aktif nitrojenaz enzimi, yedi demir atomu, dokuz kükürt atomu, bir molibden atomu ve bir karbon atomu içeren bir demir-kükürt kümesi kullanır. Bu çalışma için ise MIT ekibi, üç demir atomu, dört kükürt atomu, bir molibden atomu olan ve karbon içermeyen bir küme oluşturdu.
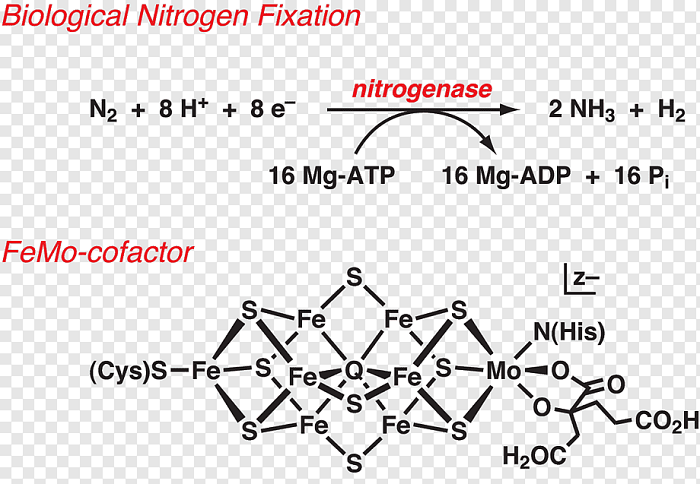
Fotoğraf-3: Biyolojik Azot Bağlanması (En aktif nitrojenaz enzimi, yedi demir atomu, dokuz kükürt atomu, bir molibden atomu ve bir karbon atomu içeren bir demir-kükürt kümesi kullanır).(4)
Moleküler azotun demir-kükürt kümesine doğal bağlanmasını taklit etmeye çalışmanın bir zorluğu, kümelerin bir çözelti içindeyken dinitrojen gibi substratları bağlamak yerine kendi aralarında reaksiyona girebilmeleridir. Bunun üstesinden gelmek için Suess ve öğrencileri, ligand adı verilen kimyasal grupları bağlayarak küme çevresinde koruyucu bir ortam yarattılar.
Araştırmacılar, N2‘ nin kümeye bağlandığı bir demir atomu dışında her bir metal atomuna bir ligand bağladılar. Bu ligandlar istenmeyen reaksiyonları önler ve N2‘ nin kümeye girmesine ve demir atomlarından birine bağlanmasına izin verir. Bu bağlanma gerçekleştiğinde, araştırmacılar X-ışını kristalografisi ve diğer teknikleri kullanarak kompleksin yapısını belirleyebildiler.
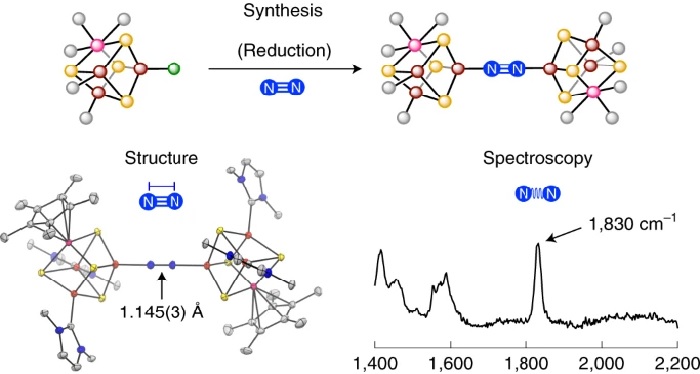
Fotoğraf-4: Molibden-demir-kükürt kümesinde N2 bağlama ve aktivasyon (3)
Ekip ayrıca, N2‘ nin iki azot atomu arasındaki üçlü bağının şaşırtıcı derecede zayıfladığını buldu. Bu zayıflama, demir atomlarının elektron yoğunluklarının çoğunu azot-azot bağına aktarmasıyla ortaya çıkar ve bu da bağı çok daha az kararlı hale getirir.
Küme İşbirliği
Bir başka şaşırtıcı bulgu, kümede yalnızca azotun bağlı olduğu demir atomunun değil, tüm metal atomlarının bu elektron transferine katkıda bulunmasıydı.
Suess, “Bu, bu kümelerin bu inert bağı etkinleştirmek için elektronik olarak işbirliği yapabildiğini gösteriyor” diyor. “Azot-azot bağı, tek başına başka bir şekilde onu zayıflatamayacak olan demir atomları tarafından küme içinde işbirliği ile zayıflatılabiliyor.”
Araştırmada yer almayan Harvard Üniversitesi Kimya ve Kimyasal Biyoloji Bölümü başkanı Theodore Betley, bulguların “demir-kükürt küme kimyasında önemli bir kilometre taşını” temsil ettiğini söylüyor.
Betley, “Atmosferik azotu dönüştüren nitrojenaz enzimlerinin, kaynaşmış demir-kükürt kümelerinden oluştuğunun bilinmesine rağmen, bugüne kadar sentetik kimyagerler bu enzimlerin yapay benzerlerini kullanarak N2 bağlanmasını, asla gösteremediler” diyor. “Bu çalışma, demir-kükürt kümesi topluluğu ve biyoinorganik kimyagerler için büyük bir ilerlemedir. Her şeyden önce, bu ilerleme demir-kükürt kümelerinin henüz keşfedilmemiş zengin bir reaksiyon kimyasına sahip olduğunu göstermiştir.”
Araştırmacıların bulguları ayrıca, demir-kükürt kümesinin bu çalışma için oluşturdukları gibi daha basit versiyonlarının da azot-azot bağını etkili bir şekilde zayıflatabildiğini doğruladı. Suess, azot sabitleme yeteneğini geliştiren en eski mikroorganizmaların da başlangıçta benzer türde basit kümeler geliştirmiş olabileceğini söylüyor.
Suess ve öğrencileri şimdi, doğal olarak oluşan demir-kükürt kümelerinin daha karmaşık versiyonlarının dinitrojen ile nasıl etkileşime girdiğini araştırıyorlar.
Kaynak: chemistry.mit.edu/news/
- https://chemistry.mit.edu/chemistry-news/how-metals-work-together-to-weaken-hardy-nitrogen-nitrogen-bonds/
- https://phys.org/news/2018-06-exploring-greener-approaches-nitrogen-fixation.html?deviceType=mobile
- Alex McSkimming, Daniel L. M. Suess. Dinitrogen binding and activation at a molybdenum–iron–sulfur cluster.Nature Chemistry, 2021; DOI: 1038/s41557-021-00701-6
- https://www.pngwing.com/en/free-png-nvjdq