Kronik Beyin Enfeksiyonunda Olayların Tamamından Sorumlu Olan Gen
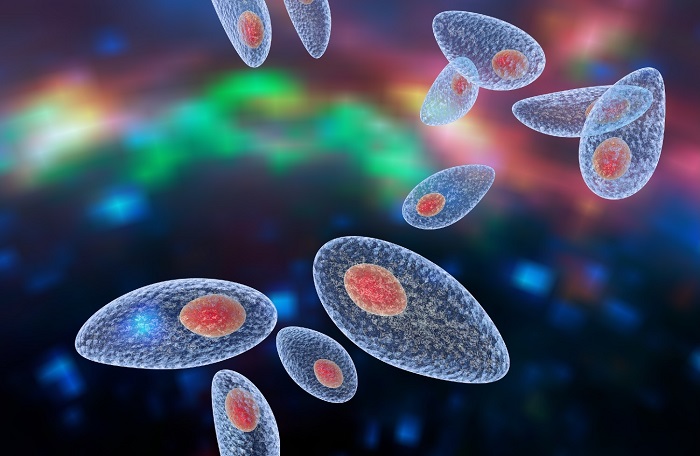
Küresel insan popülasyonunun yaklaşık üçte birinin, tek hücreli bir organizma olan Toxoplasma gondii ile (gıdalarla yutulabilen veya bahçecilik gibi aktivitelerden alınabilen bir parazit) enfekte olduğu tahmin edilmekte. Parazitin, beyin ve kas dokusunda kalıcı bir enfeksiyon oluşturmak için kronik bir aşamaya ayrılması gerekir ancak bu parazitin bu dönüşümünün nasıl gerçekleştiği bir gizem. Writing in Cell dergisine Waldman ve arkadaşları, bu farklılaşma olayının bir ana regülatörünü kodlayan bir genin kimliğini bulduklarını bildirdi.
Toxoplasma gondii herhangi bir sıcak kanlı hayvana bulaşabilir. İnsan enfeksiyonu, enfekte hayvanlardan az pişmiş et yiyerek, kontamine yiyecek veya su tüketerek meydana gelebilir. Konağına girdikten birkaç hafta sonra, T. gondii , akut evre takozoit adı verilen bir formdan, kronik bir enfeksiyon oluşturan bir bradizoite dönüşür. Bir bradyzoit, konakçı hücrelerde bulunan ve kalın bir protein -şeker duvarı ile çevrili bir kist oluşturur. Bu duvar, kisti erişilemez hale getiren ve ilaçlarla veya konağın bağışıklık sistemi ile ortadan kaldırılmasını engelleyen müthiş bir bariyerdir. T.gondii enfeksiyonu insan popülasyonlarında yaygın olmasına rağmen, genellikle zararsızdır. Hastalık aktive edilmiş takimoit formuna geri dönmeyen genellikle bradizoit formdadır. Bununla birlikte, T. gondiienfeksiyonu, doğmamış fetüsler veya bağışıklık sistemlerinden ödün verilmiş kişiler için hayati tehdittir. Ayrıca, Amerika Birleşik Devletleri’nde, T. gondii enfeksiyonlarının % 2’si tedaviye dirençli parazitlerin meydana getirdiği oküler hasar nedeniyle görme sorunları veya körlük ile sonuçlanıyor.
Bradyzoitlerin oluşumunu kontrol eden geni ortaya çıkarmak için Waldman ve meslektaşları T.gondii’ye yeşil floresan geni aktardı, eğer canlıda bu tür kistler oluşursa yeşil floresan proteini sayesinde gözlemlenebilir. Floresan proteini mikroskopi ve hücre ayırma teknolojileri kullanılarak izlenmesi, parazitin kronik enfeksiyonla ilişkili forma farklılaşıp farklılaşmadığını değerlendirmek için bir yol sundu. Kültür koşullarında strese sebep olan tedaviye maruz bırakmak örneğin alkali pH’a sahip kültür koşullarında, paraziti bradikoidlere ayırdı. Araştırmacılar, seçilen genlerin herhangi birinin farklılaşmayı etkileyip etkilemediğini değerlendirmek için CRISPR gen düzenleme aracını kullandılar. Sonuçlar çarpıcı ve netti. Sadece bir hedef genin bozulması bradizoit oluşumunu engelledi. Bu gen BFD1; Myb-alanı içeren proteinler olarak bilinen bir aileye ait transkripsiyon faktörü proteinini kodlayan bir gendir.
Waldman ve takımı BFD1’nin T . gondii’nin Myb alanında farklılaşma gösterdiğini keşfetti. Başka bir protein Myb-alanı içeren parazit olan Giardia lambia, kronik aşamalı kist oluşumunu kontrol etme özelliğiyle ilgi çekicidir. Ayrıca, protein Myb-alanı içeren türler ailesinde ilgili bir üye olan kırmızı kan hücrelerinde Plasmodium parazit’i gelişmesini sağlar. BFD1, ek olarak T . gondii ‘de diğer protein Myb- alanı içeren proteini kodlar. Bu konuda işlevlerini belirlemek ve herhangi birinin enfeksiyon sürecine yardımcı olup olmadığını belirlemek bir öncelik olmalıdır.
Waldman ve takımı BFD1 içermeyen T.gondii taşıyan farelerde kronik bir enfeksiyonun oluşmadığını gözlemledi. BFD1 ekspresyonunun düzenlenmesini araştırırken, araştırmacılar, BFD1 kodlayan haberci RNA’nın hem akut hem de kronik enfeksiyon aşamalarında benzer bir seviyede eksprese edildiğine dair bir keşifte bulundu. BFD1’in varlığı, parazit farklılaşmasına ve bradizoite forma geçmesinde yeterlidir. BFD1’i kodlayan mRNA, enfeksiyonun kronik aşaması sırasında proteine çevrilir. Bu bulgudan yararlanarak Waldman ve takımı bir mühendislik uygulaması ile T . gondii’yi spesifik bir bileşik verilmedikçe BFD1’in kararsız bir durumda olacağı bir form haline getirdiler. Araştırmacıların tasarladığı bu modele uygun olarak, BFD1’in bileşik aracılı stabilizasyonu parazitin bir bradizoit oluşturmasıyla sonuç buldu. Bu keşif, BFD1’i kodlayan mRNA’nın, muhtemelen strese yanıt olarak, kronik enfeksiyonu tetiklemek için nasıl düzenleneceği sorusunu akıllara getirdi.
Beklendiği gibi, T .gondii stresli koşullar altında (in vitro) konakçı hücrelerde birkaç replikasyondan sonra bradizoitlere farklılaşan ( in vivo) parazitlerde bu stres kısmen konakçının bağışıklık tepkisinden kaynaklanıyor. Bu işlem, kültürlenen tüm parazitler arasında ve hatta bir konakçı hücrede olanlar için senkronize değil. Bu nedenle araştırmacılar, farklılaşma olayıyla ilişkili gen ekspresyon profillerini değerlendirmek için vahşi tip ve BFD1 eksik parazitlerin tek hücreli RNA profillemesini kullandılar. Ayrıca BFD1’in bağlandığı parazit genomunun bölgelerini de araştırdılar. Bir transkripsiyon faktörünün beklendiği gibi, BFD1 transkripsiyon başlangıç yerleri olarak adlandırılan gen bölgelerine ve özellikle araştırmacıların farklılaşma sırasında normal seviyelerden daha yüksek olarak eksprese edildiğini belirledikleri geniş bir gen grubuna bağlanmıştır.
Birçok soru BFD1 farklılaşması veya gen düzenlenmesiyle ilgili ve cevapsız. Nasıl farklılaştığını bilmek önemli ancak yeterli değil. ApiAP2s denilen önceden tanımlanmış transkripsiyon faktörleri, bir grup membran hareketinde görev alıyor olabilir. BFD1’in (muhtemelen) translasyonel kontrol ile düzenlendiği düşünüldüğünde, tek hücrelerin RNA içeriğini belirleyen yaklaşımlar; farklılaşmayı tetikleyen faktörlerin tamamını tanımlamak için yeterli olmayabilir. Çeviri kontrolünü araştırmanın bir başka yolu, ribozom kompleksinin çeviri mekaniğine bağlı RNA’ları profillendirmektir. Bu yöntem zaten T.gondii için kullanılmış ve bradikoidleri incelemek içinde dahil edilmelidir.
Bradyzoitler şimdi konakçı hücreleri olumsuz etkilemeden (in vitro) olarak büyütülmüş konakçı hücrelerde tutulabilir ve gelecekteki deneyler için birçok sonuca açılabilir. Özellikle heyecan verici bir sonuç, beyin enfeksiyonu sırasında bradikzoitlerin, nöronal kök hücreleri üretmek için uygulanan kök hücre teknolojilerinde kullanan bir yaklaşımla analiz edilmesi olası. CRISPR, konakçı genlerin rolünü test etmenin bir yolunu sunar ve bu yöntem de T. Gondii’yi hem in vitro ve in vivo hedefleyebilir . Bu araçların mevcudiyeti, akut ve kronik enfeksiyon aşamaları boyunca parazit, konakçı ve bağışıklık sistemi arasındaki etkileşim hakkında yeni keşifler için ortam hazırlamaktadır. T.gondii görüntülerindeki karmaşık ve ince farklılıkların bilgisayar üzerinden değerlendirilmesini sağlayan yapay zeka yöntemlerinin geliştirilmesi, enfeksiyon sürecini değerlendirmek için başka bir yöntem sunar.
Bradyzoitlerin T.gondii ile alakalı en zorlu aşaması olduğu göz önüne alındığında; insanda hastalığın tedavisi için mücadele edilecek yaşam döngüsü, BFD1’i hedeflemek, ilaçların veya aşıların geliştirilmesinde ilerleme sağlama konusunda gerçek bir potansiyel göstermektedir. Hepsine hükmedebilecek bir genin keşfi bizi bu kronik enfeksiyonun bilmecesini çözmeye daha da yaklaştırıyor.
Kaynak: nature.com