Genetik Olarak Tasarlanmış Maya İlaçlar için Gereken Bitkisel Kimyasalları Üretebilir
Homeros’un Odyssey eserinde de büyücü Circe, Odysseus’un arkadaşlarında amnezi ve halüsinasyonları tetiklemek için bir zehir kullandı. Bilim insanları Circe’nin bu bitki karışımı (içerdiğini Datura stramonium astım tedavisinde, grip semptomları ve ağrı kesici olarak kullanılan tropanik alkaloidleri adı verilen moleküllerce zengindir), bu halüsinojenik ve diğer psikotropik etkilere neden olur. Tropan alkaloidler, diğer birçok doğal bitki ürününde olduğu gibi, hala tipik olarak doğal kaynaklardan elde edilir, ancak bu yaklaşımın da birçok gizli tehlikesi vardır. Örneğin, hava koşullarına ve piyasadaki dalgalanmalara karşı savunmasızlık, hem hastalar hem de araştırmacılar için erişimi sınırlayabilir ve yapılan ekstraksiyon çevreye zararlı olabilir. Ek olarak, bitkiler tipik olarak bu aktif bileşenleri çok düşük seviyelerde içerir. Nature Dergisine yazan çalışmada araştırmacı olan Srinivasan ve Smolke , ekmek mayası olan Saccharomyces cerevisiae’nin genetik olarak tasarlanmış suşlarını kullanarak bu sınırlamaları hafifletebilecek tropan alkaloidler üretmenin alternatif bir yolunu bizlerle paylaştı.
Bitkiler, uyum sağlamalarına ve hayatta kalmalarına yardımcı olan çeşitli özel bileşikler üretir. Bu doğal ürünlerin biyosentezi genellikle karmaşık dinamikleri ve düzenlemeleri olan uzun metabolik yollar içerir. Metabolik mühendisliği alanında önemli başarılarından biri “bitkilerin ürettiği doğal ürünleri üretebilir mikroorganizmaların geliştirilmesi” olmuştur. Bununla birlikte, bu yaklaşım rutin olmaktan uzaktır çünkü biyosentezde yer alan enzimler genellikle bilinmemektedir veya mikrobiyal konakçılarda bu maddeler inaktif olabilir hatta bitkinin farklı alt hücresel bölmelerinde üretilebilen ya da hücreler-dokular arasında farklılıklar gösteren bir durumda olabilir.
Srinivasan ve Smolke ; basit şekerleri ve amino asitleri, iki tropan alkaloid, hyoscyamine ve scopolamine dönüştüren bir S. cerevisiae türü üretmek için bu zorlukların üstesinden gelindiğini belirttiler. Bu tropan alkaloidler; nörotransmiter molekülü asetilkolin’in etkisini bloke eder. Bulantı, mide-bağırsak sorunları, aşırı vücut salgıları ve Parkinson hastalığının da dahil olduğu birçok nöromüsküler bozuklukları tedavi etmek için kullanılırlar.
Srinivasan ve Smolke, farklı Kingdomdan(taksonomik basamak) 26 geni ekspers etmek için maya suşlarını genetik olarak tasarladılar. Bu genler birlikte, çeşitli metabolik enzimleri ve taşıyıcı proteinleri kodlar. Araştırmacıların başarısının anahtarı, enzimleri ve taşıyıcıları 6 hücre altı bölgeye ayırmalarıdır (sitozolik sıvı, dört organel (mitokondri, peroksizom, vakuol ve endoplazmik retikulum) ve vakuolar membranlar). Enzimlerin hücre altı bölmelere ayrılması, uygun enzimatik aktiviteyi sağlayarak ve metabolik ara maddeleri izole ederek toksisitelerini ve rakip yollarda kayıplarını azaltarak ürün biyosentezini iyileştirebilir. Alanı kısıtlayarak, bölmelere ayırma enzimler ve hedefleri arasındaki yerel etkileşimleri de artırır. Bu nedenle enzimlerin bu şekilde ayrılması, farklı reaktörlerde farklı sentez aşamalarının yürütüldüğü (kimyasal fabrikalarda olanlara benzer) bu nedenlede her aşama, üretkenliği en üst düzeye çıkarmak için ayrı ayrı optimize edilebilir.
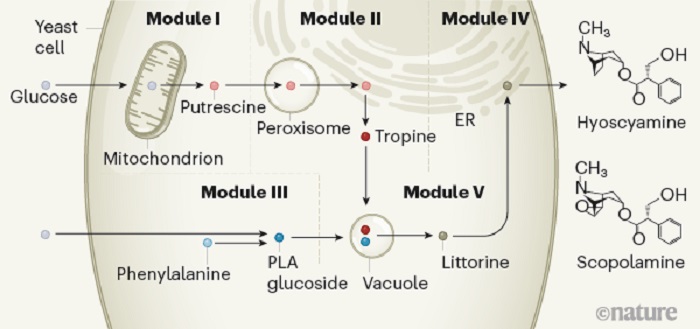
Araştırmacılar, hyoscyamine ve scopolamine için biyosentetik yolu beş modüle böldüler (Görsel1), bunlardan ilk ikisini geçen yıl yayımlanan çalışmada anlattılar. Örneğin modül I’de, glikozdan türetilen amino asit glutamat, kısmen mitokondride meydana gelen bir dizi reaksiyonda başka bir amino asit olan arginin’e dönüştürülür. Arginin daha sonra sitozolde putrescine dönüştürülür. Modül II’de, putrescine, biri peroksizomda katalize edilen ve diğeri endoplazmik retikulumun zarına tutturulmuş bir enzim tarafından katalize edilen birkaç sitozolik reaksiyonla, tropan alkaloidler adını veren fonksiyonel ve ana bir birleşik olan tropine dönüştürülür.
Fotoğraf : Mayada tropan-alkaloit molekülleri üretmek.
Srinivasan ve Smolke, Saccharomyces cerevisiae mayasını; hiyosiyamin ve skopolamin ilaçlarının üretimi için glikoz ve amino asitlerden üretebilmek için tasarladı. Biyosentetik yolları beş modüle bölünmüş ve birkaç reaksiyonu zara sahip ve bağlı organellerle sınırlandırmışlardır. Modül I’de glikoz, mitokondri ve sitozolik sıvıda metabolik adımlarla molekül putresine dönüştürülür. Modül II’de, peroksizomdaki ve endoplazmik retikulum (ER) zarındaki enzimatik reaksiyonlarla bu putresinin tropine dönüşümünü katalize eder. Modül III’te (modül I ve II’ye paralel olarak oluşur), glikoz ve amino asit fenilalanin fenillaktik asit glukosite (PLA glukozit) dönüştürülür. Modül V’te, tropin ve PLA glukozit, vakuole taşınır ve birlikte littorine dönüştürülür. Son olarak, bir kısmı ER membranında oluşan modül IV’te, littorin hyoscyamine dönüştürülür.
Modül III, sitozoldeki modül I ve II ile paralel olarak oluşur ve glikozu, amino asiti fenilalanini molekül fenilaktik asit glukozidine (PLA glukozid) dönüştürür. Bu modül için araştırmacılar, ölümcül olan Güzelavrat otu olarak bilinen Atropa belladonna’da bitkisinde bulunan ve PLA glukozit üretimini katalize eden PLA UDP-glukosiltransferaz adlı bir enzimi ifade edecek şekilde kendi suşlarını tasarladılar.
Modül II’de üretilen tropin ve modül III’teki PLA glukozid, vakuole aktarılır. Daha sonra, modül V’de (tüm unsurları yeni keşifler oluşturduğu için tahminsel olarak en son numaralandırılır), tropin ve PLA glukozit, littorin molekülüne dönüştürülür. Yapı modülü V iki temel adım içeriyor. İlk olarak, Srinivasan ve Smolke Nicotiana tabacum’da süzgeçten geçirerek hızlı bir şekilde tropine’ı vokuole taşıyıcak bir proteini ekspre etmek için çeşitli suşlar tasarladılar. İkinci olarak, hücreleri A. Belladonna’da enzim olan littorin sentazın ( Ab LS) bir varyantını ekspre edecek şekilde tasarlandı. Mayayla ekspres edildiğinde AbLS, trans-Golgi ağında (Trans Golgi Network; Golgi adlı organelin parçası) durur ve bu nedenle vakuolar littorin üretimini katalize edemez. Bu nedenle araştırmacılar, Ab LS’yi bir transmembran proteini olacak şekilde tasarladılar (bu proteinler, varsayılan olarak alınmıştır) TGN’den vakuole taşınır. Bu Ab LS varyantı, vakuolde littorin üretimini katalize edebilir.
Yolun son adımı, modül IV, kısmen endoplazmik retikulum zarında meydana gelir. Bu modülde, littorin hyoscyamine ve ardından skopolamine dönüştürülür. Hyoscyamin üretimindeki son adım, hyoscyamin dehidrogenaz (HDH) enzimini içerir, ancak bu enzimi kodlayan gen bilinmiyordu. Araştırmacılar, 12 aday gen oluşturmak için A. belladonna’dan gen ekspresyon profillerinin bir veri setini analiz ettiler. Hangisinin istenen enzimatik aktiviteye sahip olduğunu belirlemek için bu adayların her birini maya suşlarında ekspre ettiler. Daha sonra A. belladonna’dan HDH-kodlayan genin aktivitesini diğer bitkilerden gelen eşdeğerlerle karşılaştırdılar ve son olarak Circe’nin Boruçiçeğini hyoscyamine ve scopolamine üretimi için genetik anlamda optimal olarak belirlediler.
Bu adımların yanı sıra, Srinivasan ve Smolke, önemli ara metabolit moleküllerini tüketen S. cerevisiae’ye özgü enzimleri ortadan kaldırdı ve biyosentetik yolun gerektirdiği metabolitlerin üretimini arttırmak için diğerlerini fazlaca ekspre etti. Birlikte yaptıkları bu çalışma, mikrobiyal platformların ilaç üretmenin daha ucuz, daha hızlı, daha güvenilir ve daha sürdürülebilir araçlarını sağlama potansiyelini gösteren büyük bir başarıdır. Onların maya suşu, maya kültürünün litresi başına sadece birkaç mikrogram ila miligram tropan alkaloid üretebildi, henüz bitki ekstraksiyonu yöntemi mevcut üretim yöntemlerimizin yerini almak için yeterli değil. Bununla birlikte, bu çalışma hedefimiz için önemli bir temel taşı.
Üretimi daha da artırmak için; bir kimya fabrikasında her reaksiyon optimize edileceğinden, yolun her modülünü optimize etmek gerekecektir. Bu, doğal enzimleri düzenleyerek veya azaltarak, hücre altı bölmeler arasında metabolit taşınmasını artırarak ve metabolik modüllerdeki enzimlerin aktivitesini iyileştirerek (daha hızlı bir biyosentezi engelleyen yoldaki anahtar adımlar) tropan-alkaloid biyosentez oranını artırmak mümkün olacaktır.
İleriye dönük olarak, araştırmacılar Srinivasan ve Smolke’nin biyosentetik yolunun olası permütasyonlarını keşfetmeli. Belki de sentezin yolundaki varyasyonlar, etkinliği artıran ve yan etkileri azaltan yeni ilaçların keşfedilmesine yol açabilir. İlerleyen dönemlerde bu yöntemlerle diğer rahatsızlıkları tedavi etmek için ilaçlar bile bulunabilir.
Kaynak : nature.com