Bu Araştırma Su Ayırıcı Katalizörler için Yeni Bir Tasarım Prensibi Sunuyor
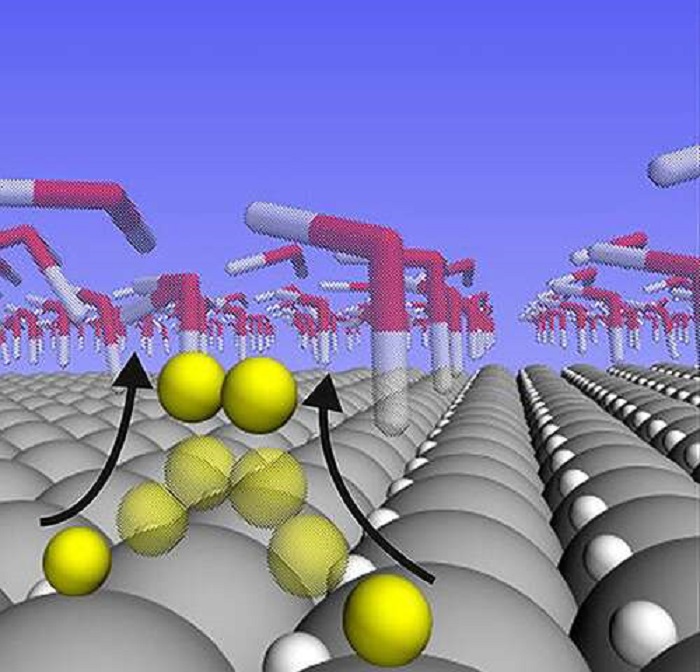
Fotoğraf: Yeni bir çalışma, su ayırma reaksiyonunda hidrojen atomlarının platin katalizörünün yüzeyinde gevşek bir şekilde bağlandığını ve oldukça hareketli olduğunu göstermektedir. Bulgular, platinin bu özel reaksiyonu katalizlemede neden bu kadar iyi olduğunu anlamaya ve platinden daha ucuz ve daha bol olan malzemelerden yapılmış katalizörlerin tasarımına yardımcı olabileceğini açıklıyor. (Kaynak: Peterson Lab / Brown Üniversitesi)
Su moleküllerinin ayrıştırılarak hidrojen gazı üretilmesinde platinin en iyi katalizör olduğu bilim insanları tarafından uzun süre biliniyor. Brown Üniversitesi’ndeki araştırmacılar tarafından yapılan yeni bir araştırmada platinin neden bu kadar iyi çalıştığı kanıtlandı.
Yazarlar ACS’de yayımlanan çalışmalarının neredeyse yüz yıllık bir sorunun çözümüne yardımcı olduğunu söylüyor ve hidrojen üretiminde platinden daha ucuz ve daha çok bulunan yeni katalizörlerin tasarlanmasının önünü açacağını düşünüyor. Bunun sonucunda da fosil yakıtların sebep olduğu emisyonların azalacağını öngörüyorlar.
Brown Üniversitesi Mühendislik Fakültesi’ndeki Profesör Andrew Peterson “Hidrojenin ucuz ve verimli bir şekilde nasıl üretebileceğimizi anlayabilirsek fosil içermeyen yakıtların ve kimyasalların önünü açabiliriz” dedi.
“Hidrojen yakıt hücrelerinde kullanılabilir, bunun için CO2 veya amonyak ve gübre elde etmek için azotla birleştirilir. Hidrojen ile yapabileceğimiz çok şey var ancak ölçeklenebilir bir hidrojen kaynağı tasarlamak için daha ucuz bir katalizöre ihtiyacımız var. Yeni katalizörler tasarlamak platini bu reaksiyon için neyin özel kıldığını anlamakla başlar” diyor Peterson ve yeni araştırmanın amacının bu olduğunu savunuyor.
Platinin başarısı uzun zamandır “Goldilocks” bağlayıcı enerjisine atfedildi. İdeal katalizörler ne çok gevşek ne de çok sıkı, ortada bir yerde reaksiyona gire moleküllere dayanır. Moleküllere çok gevşek bir şekilde bağlandıklarına reaksiyona başlamak oldukça zordur. Çok sıkı bağlandıklarında moleküller katalizörün yüzeyine yapışır ve reaksiyonun tamamlanması zorlaşır. Hidrojenin platin üzerindeki bağlanma enerjisi su ayırıcı reaksiyonun iki bölümünü mükemmel bir şekilde dengeler ve platini mükemmel yapan şey de budur.
“Ancak, bu resmin doğru olup olmadığını sorgulamak için nedenler vardı” diyor Peterson. Örneğin, molibden disülfür adı verilen bir malzeme platine benzer bir bağlama enerjisine sahiptir. Ancak, su ayırma reaksiyonu için daha kötü bir katalizördür.
Peterson ve meslektaşları neler olduğunu öğrenmek için elektrokimyasal reaksiyonlardaki her bir atomun ve elektronun davranışını simüle etmek için geliştirdikleri özel bir yöntem kullanarak platin katalizörünün su ayırma reaksiyonu üzerindeki etkilerini inceledi.
Analizleri “Goldilock” bağlanma enerjisindeki platinin yüzeyine bağlanan hidrojen atomlarının, reaksiyon hızı yüksek olduğu zaman reaksiyona katılmadıklarını göstermiştir. Bunun yerine bu atomların kristal platinin yüzeyine yerleştiğini gözlemlediler. Reaksiyona katılan hidrojen atomları “Goldilocks” enerjisinden çok daha zayıf bir bağlanma göstermiştir. Kristal örgünün içine yerleşmek yerine hidrojen gazı oluşturmak için platin atomlarının üzerinde yerlerini alırlar.
Araştırmacılar platini bu kadar reaktif hale getiren şeyin yüzeydeki hidrojen atomlarının hareket özgürlüğü olduğunu sonucuna varıyor.
Peterson “Bu sonucun bize söylediği şey bu “Goldilocks” bağlayıcı enerjisini incelemenin yüksek aktivite bölgesi için doğru bir tasarım ilkesi olmadığıdır. Hidrojeni bu son derece hareketli ve reaktif hale getiren katalizörlerinin tasarlanmasının başka yolları olduğunu savunuyoruz” diyor.
Kaynak: phys.org