Antoine-Laurent de Lavoisier
Lavoisier, 26 ağustos 1743’te varlıklı bir ailenin bireyi olarak Paris’te doğdu. Paris Parlanmetosu’ndaki bir vekilin oğlu olan Lavoisier, annesinin ölümü ile birlikte beş yaşındayken büyük bir mirasa sahip oldu. 11 yaşında (1754) Paris’teki Dört Ulus Koleji’ne (Mazarin Koleji olarak bilinir daha çok) başladı. Okulun son iki yılında (1760-1761), bilim merakı canlandı ve Kimya, Botanik, Astronomi ve Matematik eğitimi aldı. Felsefe sınıfında Abbé Nicolas Louis de Lacaille’in vesayeti altına girip, seçkin bir matematikçi ve gözlemci gökbilimci olan genç Lavoisier, meteorolojik gözlem merakını kendisini hiç terk etmeyen hevesiyle telkin etti. Babasının yerini alma isteğiyle başladığı Hukuk okulundan 1763’te lisans derecesi aldı ve 1764’te de mezun oldu. Lavoisier hukuk diplomasını aldı ve baroya kabul edildi ama bir avukat olarak hiç çalışmadı. Belli başlı boş zamanlarında bilim eğitimine devam etti.
Lavoisier’in eğitimi, Fransız Aydınlanmasının idealleri ile doluydu ve Pierre Macquer’in Kimya sözlüğüne hayrandı. Doğa bilimleri konferanslarına katıldı. 18. yüzyılın ünlü Fransız bilim insanı olan Étienne Condillac, Lavoisier’in Kimya’ya olan bağlılığı ve tutkusu üzerinde epey etki etti. İlk Kimya yayını 1764’te gerçekleşti. 1763-1767 yılları arasında Jean-Étienne Guettard bünyesinde jeoloji eğitimi aldı. Gutterd ile işbirliği yaparak Haziran 1767’de Alsace-Lorraine’in jeoloji i ölçümü üzerine çalıştı. 1764’te alçıtaşının (Hidratlı kalsiyum sülfat) kimyasal ve fiziksel özellikleri üzerine olan makalesi ilk kez Fransa’nın en seçkin bilim topluluğu olan Fransız Bilimler akademisinde okundu ve 1766’da Şehrin sokak aydınlatmasının sorunlarındaki girişimi için Kral kendisine altın madalya verdi. 1768 yılında Bilimler Akademisine geçici göreve tayin edildi. 1769’da Fransa’nın ilk jeolojik haritası üzerinde çalıştı.
Bilimler Akademisine suyun buharlaşma ile yeryüzüne düştüğü ile ilgili bir inceleme yazısı sundu. Lavoisier, çok hassas kantitatif deneyle bir cam kabın içindeki suyun uzun süre devam eden ısıtmayla geri akışından sonra üretilen “toprağımsı” tortunun, suyun yeryüzüne dönmesinden değil, daha çok cam iç yüzeyine kademeli olarak dağılmasından kaynaklandığını gösterdi.
1772 yılının sonlarında Lavoisier, bilim üzerindeki en önemli katkı yaptığı konu dikkat çektiği yanma olayıdır. İlk deney sonuçlarını 20 Ekim’de Akademi’ye bir dosya halinde sundu ve burada fosforun yakıldığında fosforlu tiner asidini üretmek için çok miktarda havayla birleştiğini ve fosforun yanma şiddetini yükselttiğini gösterdi. Birkaç hafta sonra ( 1 Kasım) Akademiye mühürlü olarak bırakılan ikinci bir dosya da, Lavoisier gözlem ve sonuçlarını kükürt yanmasıyla genişletti ve şunları dosyaya ekledi “ Kükürt ve Fosfor’un yakılmasında gözlemlenen şey, yanma ve kalsinasyonda ağırılığı yükselen tüm maddelerdurumunda gerçekleşebilir: Metalik kalsiyum oksitin ağırlığındaki artışın aynı sebepten kaynaklandığına ikna oldum.”
1773 süresince Lavoisier, hava ile ilgili literatörü özellikle “sabit havayı” iyice gözden geçirmeye ve bu alanda çalışan diğer çalışanların deneylerinin çoğunu tekrarlamaya karar verdi. Bu gözden geçirmenin hesabını 1774’te Opuscules physiques et chimiques ( fiziksel ve kimyasal denemeler) ismindeki bir kitapta yayımladı. Bu inceleme sırasında hafif ve kostik alkaliler üzerinde klasik nicel deneyler serisini gerçekleştiren İskoç kimyacı Joseph Black’in çalışmasına ilişkin ilk kez tam bir çalışma yaptı. Black, yumuşak bir alkali; örneğin tebeşir (CaCO3) ve aşındırıcı (kostik) biçimi olan sönmemiş kireç (CaO) arasındaki farkın gerçekte öncekinin “sabit hava” içerdiği gerçeğinden yola çıkıldı sabit havadaki tebeşirden bahsetmedi ancak atmosferin bir unsuru olan Karbondioksitin (CO2) belirgin bir kimyasal olduğu şimdilerde anlaşıldı. Lavoisier Black’in sabit havasının, metal kalsiyum oksitin kömürle indirgendiği zaman ortaya çıkan hava ile aynı olduğunu fark etti ve hatta kalsinasyon sırasında metallerle birleşen ve ağırlığı arttırabilen havanın Black’in sabit havasının yani CO2 olduğunu öne sürdü.
1774 ilkbaharında Lavoisier, kapalı kaplarda kalayın ve kurşunun kalsinasyonu üzerine deneyler yaparak metallerin ağırlığındaki artışın yanmadaki hava ile birleşiminden kaynaklandığını kesin olarak doğruladı. Fakat bunun ortak atmosfer havasıyla mı yoksa sadece atmosferik havanın bir kısmıyla birlikte kaldığı sorusu kaldı. Ekim ayında İngiliz Kimyager Joseph Priestley, Paris’i ziyaret Lavoisier ile tanıştı ve kendisine ürettiği havayı cıvalı kırmızı renkli dumanı yanan bir camla ısıtırak ve aşırı derecede yanmayı destekleyen havadan bahsetti. Priestley, bu gazın doğasından emin değildi ancak bunun özellikle saf bir hava çeşidi olduğunu hisetti. Lavoisier bu garip madde üzerine kendi araştırmalarını yaptı. Sonuç, Kalsinasyon sırasında Metallerle Birleşen ve Ağırlığını Arttıran İlke Hakkındaki inceleme yazısı 26 Nisan 1775’te Akademide okundu (yaygın olarak Paskalya Anısı olarak anılacaktır). Lavoisier orijinal dosyasında, cıva kalsiyum oksitin, gerçek bir metalik kalsiyum oksitin kömür ile indirgenmesiyle oluştuğunu gösterdi ve proseste Black’in sabit havasını verdi. Kömür olmadan indirgendiğinde gelişmiş bir yöntemle solunum ve yanmayı destekleyen hava verdi. Bunun sadece saf bir hava çeşidi olduğunu ve havanın kalsinasyonda metaller ile birleştiğinde “parçalanmadan, ayrışmadan, değişmeden” havaya karıştığına karar verdi. Paris’ten döndükten sonra Priestley, havadaki cıva kalsiyum oksit incelemesini bir kez daha ele aldı. Sonuçları, bu havanın yalnızca saf bir hava çeşidi olmadığını ancak “solunum, iltihaplanma ve diğer her şeyde ortak hava kullanımı için ortak havadan beş veya altı kat daha iyi” olduğunu gösterdi. Flogiston’dan mahrum kalan ortak havanın olduğunu düşündüğü havada oksijen gazını aradı. Bundan dolayı, yanan cisimler ve solunan hayvanlar tarafından verilen daha büyük miktarda flogistonu absorbe edebilen bir duruma sahip olduğu için maddelerin daha fazla yanması ve bu havadaki solunum kolaylığının önemli kısmı açıklandı.
Lavoisier’in araştırmaları, ilk gerçek kantitatif kimyasal deneylerin bazılarını içermektedir. Herhangi bir gazın kaçamayacağı, kimyanın ilerlemesinde çok önemli bir adım olan, kapalı bir cam kabın içinde reaktanları ve kimyasal tepkimelerin ürünlerini titizlikle tarttı. 1774’te madde, kimyasal reaksiyonda durumunu değiştirebilirse de, her kimyasal değişimin başlangıcında toplam maddenin kütlesi sonunda aynı olur. Örneğin, bir odun külüne kadar yakılırsa, gaz halindeki reaktifler ve ürünler dahil edilirse toplam kütle değişmeden kalır. Lavoisier’in deneyleri kütlenin korunumu yasasını destekledi. Fransa’da Lavoisier’in yasası olarak öğretilir ve “Traité Élémentaire de Chimie”(Kimya Temel Antlaşması) de “Rien ne se perd, rien ne se crée, tout se transforme”(Hiçbir şey kaybolmaz, hiçbir şey yaratılmaz, her şey değişir) den bir açıklama yapılır. Mikhail Lomonosov (1711-1765), benzer düşünceleri daha önce 1748’de ifade etmiş ve deneylerle kanıtlamıştır; Lavoisier’in eserleri Jean Rey (1583-1645), Joseph Black (1728-1799) ve Henry Cavendish (1731-1810) gibi eserlerinde öne çıkıyor.
Lavoisier, Louis-Bernard Guyton de Morveau, Claude-Louis Berthollet ve Antoine François de Fourcroy ile birlikte, 1787’de Akademiye kimyasal isimlendirme reformları için yeni bir program sundu çünkü bu konuda neredeyse rasyonel hiç bir kimyasal adlandırma sistemi yoktu o zaman. Metod isimlendirmesi (Kimyasal Adlandırma Yöntemi, 1787) başlıklı bu çalışma, Lavoisier’in yeni kimyasındaki oksijen teorisinin ayrılmaz bir parçası olan yeni sistemi tanıttı.
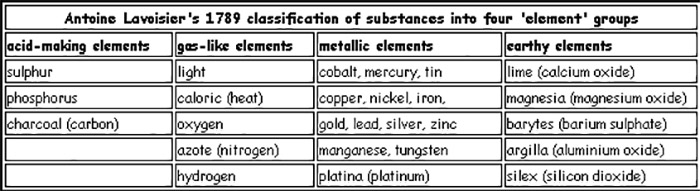
Toprak, hava, ateş ve su olan klasik elementler atıldı ve bunun yerine bilinen kimyasal yollarla daha basit maddelere dönüştürülemeyen 55 madde geçici elementler olarak listelendi. Elementler ışık içermekteydi; kalorili (ısı maddesi); oksijen, hidrojen ve azot prensipleri; karbon; sülfür; fosfor; Mürik asit (hidroklorik asit), borik asit ve “florik”asitin henüz bilinmeyen “radikalleri”; 17 metal; 5 toprak (magnezyum, barit ve stronti gibi henüz bilinmeyen başlıca metallerin oksitleri); üç alkaliler (potas, soda ve amonyak); ve 19 organik asit “radikali”. Yeni sistemde çeşitli elementlerin oksijenli bileşikleri olarak kabul edilen asitlere, söz konusu elementin oksijenasyon derecesi ile birlikte bulunan elementi, örneğin sülfürik ve sülfürlü asitleri fosforik ve fosforlu asitleri, nitrik ve azotlu asitleri, “ik” ile biten, “lu” ile bitenlere oranla oksijen oranının yüksek olduğu asitleri belirtir. Benzer şekilde “ik” asitlerin tuzlarına bakır sülfatta olduğu gibi “at” terminal harfleri verilirken “lu” asitlerinin tuzları bakır sülfitte olduğu gibi “it” sonekiyle son bulur. Yeni adlandırmanın toplam etkisi, yeni adı “bakır sülfat” ile eski “Venüs çürüğü” terimini karşılaştırarak ölçülebilir. Lavoisier’in yeni terminoljisi Avrupa’da ve Amerika Birleşik Devletleri’nde yayılmış ve kimya alanında ortak kullanıma kavuşmuştur. Bu, bilim dalına anti-flogistic yaklaşımın başlangıcı oldu.
Lavoisier, kimyasal devrimde katkı sunanların merkezinde olduğu için adından sıkça bahsedilmektedir. Hassas ölçümleri ve deneyleri boyunca titizlikle bakılan sonuçlar, kütlenin korunumu yasasının genişçe kabul görmesi için yaşamsal önem taşıyordu. Linnaeus’tan sonra modellenen binom (iki terimli) sistemi olan yeni terminolojiye girişi, alanda genellikle kimyasal devrim olarak anılan dramatik değişiklikleri işaretlemeye de yardımcı oluyor. Bununla birlikte Lavoisier, özellikle İngiliz flogistik bilim insanlarını değiştirmeye çalışırken çok fazla muhalefetle kaşılaştı. Joseph Priestley, Richard Kirwan, James Keir ve Williaam Nicholson, diğerlerinin yanı sıra maddelerin niceleştirilmesinin kütle korunması anlamına gelmediğini savundu. Muhalefet, gerçek kanıtları rapor etmek yerine, Lavoisier’in yaptığı araştırmanın sonuçlarını yanlış yorumladığını iddia etti. Lavoisier’in müttefiklerinden Jean Baptiste Biot, Lavoisier’in metodoljisini şöyle yazdı: “deneylerde doğruluk ile mantık kurallarının birbirine bağlanmasının gerekliliğini hissediyordu.” Ancak muhalefeti, deneydeki hassaslığın, çıkarsamalar ve akıl yürütme konusunda kesin bir şey ifade etmediğini belirtti. Lavoisier muhalefete rağmen diğer kimyagerleri, sonuçlarını beş ile sekiz ondalık basamağa kadar sonuçlandırmaya ikna etmek için dakik/kesin aleti kullanmaya devam etti. Bu ondalık basamakların sadece üçünün anlamlı olduğunu tahmin eden Nicholson, şunları söyledi:
Bu sonuçların son rakamlarında doğru gibi davranıldığı inkar ediliyorsa bazı durumlarda deneylerin bin katına kadar uzanan bu uzun rakam dizilerinin yalnızca gösterişe hizmet ettiğini, gözlemlemeye gerçek bilimin gösteriş sunmaya ihtiyacı olmadığını: ve bundan da ötesi, deneylerdeki gerçek doğruluk derecesi seyrimizden gizlendiğinde, deneylerin kesin doğruluğunun aslında delilleri inandırıcılık kimliğiyle buluşturup oluşturmamıza kuşku uyandırır.
Lavoisier’in Paskalya Anısının “resmi” hali 1778’de ortaya çıktı. Araya giren dönemde Lavoisier, Priestley’nin en son deneylerinin bazılarını tekrarlamak ve kendi yenilerini yapacak yeterli zamanı vardı. Priestley’nin oksijenli havasını (dephlogisticate air) incelemenin yanı sıra metallerin kalsine edildiğinde tortulaşan havayı daha iyi inceledi. Bu tortulaşan havanın ne yanmayı ne de solunumu desteklemediğini ve bu havanın yaklaşık beş hacminin oksijenli havanın bir hacmine eklendiğinde genel atmosferik havayı verdiğini gösterdi. Atmosferik hava, oldukça farklı özelliklere sahip iki farklı kimyasalın karışımından oluşuyordu.
Böylece Paskalya Anısı’nın revize edilmiş hali 1778’de yayımlandığında Lavoisier, artık kalsinasyonda metaller ile birleşen ilkeyi sadece genel hava olduğunu fakat “havanın en sağlıklı ve en saf olan kısmı hariç” ya da “ seçici olarak solunabilir havanın parçası” olarak tanımladı. Aynı yıl havayı meydana getiren bu madde için oksijen adını, “asit öncüsü” anlamına gelen Yunanca kelimelerden aldı. Kükürt, Fosfor, Kömür ve Azot gibi ametal ürünlerin asitli olduğu gerçeğiyle karşılaştı. Tüm asitlerin oksijen içerdiğini ve bu nedenle oksijenin asitleştirme prensibi olduğunu savundu.
Lavoisier’in 1772-1778 yılları arasındaki kimya araştırması büyük ölçüde yeni yanma teorisini geliştirmeyle ilgiliydi. 1783’te akademinin ünlü raporunda Réflexions sur le phlogistique (Flogistonda yansımalar) adlı konusunu, flogiston yanma teorisine tam boyutlu bir saldırı olarak yorumladı. O yıl Lavoisier, yanma teorisinin önemli bir öncülünü ispatladı ve teorisine pek çok dönüştürmeyi kazandıran su bileşimi üzerine bir dizi deney başlattı. Birçok araştırmacı, gazların elektrikle kıvılcım çıkaran karşımları, Henry Cavendish’in parlayıcı havası ile Lavoisier’in hidrojen (Yunanca da “su oluşturucu”) olarak adlandırdığı yanıcı havanın kombinasyonu ile denemeler yaptılar. Araştırmacılar, suyun üretimini not aldılar ancak hepsi reaksiyonu, flogiston teorisi çerçevesinde çeşitli şekillerde yorumladı. Lavoisier, matematikçi Pierre Simon de Laplace ile işbirliği yaparak cam fanus içinde cıva üzerinde hidrojen ve oksijen jetleri yakarak su sentezledi. Niceliksel sonuçlar, suyun 2 000 yıldan beri düşünüldüğü gibi bir element olmadığı ancak iki gazın bileşiminden oluştuğu görüşünü destekleyecek kadar iyi idi. Suyun bir bileşik olarak yorumlanması, metalleri asitte (su ayrıştığında üretilen hidrojen) eriterek ve indirgenmiş kalsiyum oksit (kalsiyum oksit gazının bileşimi ile oksijenden suyun oluşumu) ile oluşan yanıcı havayı açıklar. Bu deneylere rağmen Lavoisier’in antiflojistik yaklaşımı birçok kimyager tarafından kabul görmedi. Lavoisier, suyun bileşimini kesin olarak kanıtlayan teorisini sürdürmek için emekli oldu. Jean-Baptiste Meusnier ile birlikte çalışan Lavoisier suyu, sıcak kırmızı demir tüfek namlusundan geçirerek demirin oksijen ile oksitlenmesi ve hidrojenin borunun ucundan ortaya çıkmasını gözlemledi. Nisan 1784’te, su kompozisyonu hakkındaki bulgularını Académie des Sciences’a (Bilim akademisi) sunarak rakamlarını sekiz ondalık basamak olarak bildirdi. Muhalifler, Lavoisier’in yanlış sonuçları göstermeye devam ettiğini ve deneyini metalle suyun bileşiminden flogiston demire kaydırdığını belirterek bu yeni deneye karşı çıktılar. Lavoisier; tümü kalibre edilmiş pnömatik bir çukur, bir dizi dengeleyici, bir termometre ve bir barometre kullanarak yeni bir alet geliştirdi. Otuz bilgin, Lavoisier’in teorilerinin doğruluğuna ikna edilmek için bu aygıtı kullanarak suyun ayrışma ve sentezine tanıklık etmeye davet edildi. Bu gösteri, suyun oksijen ve hidrojen bileşiği olarak görülmesini sağlayan kişiler için büyük bir kesinlik kazandı. Bununla birlikte, deneyin yaygınlaştırılması, ölçümlerde hassaslık oranını detaylı bir şekilde gözlemlemek için gerekli ayrıntılar olmadığı için olması gerekenden daha az kanıtlandı. Raporun sonunda suyun bileşiminin “teklifin keskinliğini ortadan kaldırmak için fazlasıyla yeterli” olduğuna dair aceleci bir ifade kullanıldı ve deneyde kullanılan yöntemin kimya ile diğer fizik bilimleriyle birleştirileceğini ve buluşları ilerleteceğini belirtti.
Lavoisier, 1789’da Traité élémentaire de chimie’de( Kimyadaki Temel İncelemeler) yayımlanan yeni terminolojiyi kullandı. Bu eser, Lavoisier’in kimyaya olan katkısının sentezi ve bu konudaki ilk modern ders kitabı olarak kabul edilebilir. Çalışmanın özü oksijen teorisiydi ve iş, yeni öğretilerin aktarımı için en etkin araç haline geldi. Kimya teorilerinin birleşik görüşünü sundu, kütlenin korunması yasasının açık ifadesini içeriyordu ve flogistonun varlığını inkar ediyordu. Bu yazının aslı, bilinen element kavramını herhangi bir kimyasal analiz yöntemiyle parçalanamayan bir madde olarak açıkladı ve Lavoisier’in elementlerden kimyasal bileşiklerin oluşum teorisini içeriyordu. Bilim tarihinde bir klasik olarak yer aldı. Zamanın önde gelen birçok kimyageri Lavoisier’in yeni fikirlerini kabul etmeyi reddettiyse de Edinburgh’ta ders kitabı olarak Traité élémentaire için talebi, Fransızca yayımından yaklaşık olarak bir yıl sonra İngilizce’ye çevirmek için yeterliydi. Her durumda, Traité élémentaire gelecek nesilleri ikna etmek için yeteri sağlamlığa sahipti.
Yanma ile solunum arasındaki ilişki, havanın her iki proseste oynadığı önemli rolü uzun zamandır kabul edilmişti. Bu nedenle Lavoisier yeni yanma teorisini solunum fizyolojisi alanına dahil etmek zorunda kaldı. Bu konuyla ilgili ilk anıları 1777’de Akademi Bilim Okulu’nda okundu ancak bu alandaki en önemli katkısı 1782/1783 kışında Laplace ile birlikte yapıldı. Sonuç olarak bu çalışma ünlü bir anı olan “On Heat”de yayımlandı. Lavoisier ve Laplace, yanma ve solunum sırasında verilen ısı miktarını ölçmek için bir buz kalorimetri cihazı tasarladı. Kalorimetrinin dış kabuğu buzla dolu iç kabuğun etrafında 0 ° C’lik sabit sıcaklığı korumak için eritilen karla doldu. Bu cihazın içine canlı bir hayvan denek kapatılıp üretilen ısı ve karbon dioksit miktarı ölçülerek ve buz kalorimetrisinde yeterli karbonun yakıldığı zaman üretilen ısı miktarını denekin ekshale edildiği miktarda karbon dioksit üretmek üzere karşılaştırarak solunumun aslında yavaş bir yanma işlemi olduğu sonucuna varmışlardır. Lavoisier, “solunumun yanması”nı yani solunum, gaz alışverişi olan mum benzeri yanmasını bekliyordu. Akciğerlerde gerçekleştiği varsayıldığı bu sürekli yavaş yanma, hayvanın vücut sıcaklığını çevrenin sıcaklığının üstünde tutmasını ve böylelikle şaşırtıcı şekilde olağanüstü hayvan ısısını ortaya koymasını sağladı. Lavoisier, 1789-1790’da Armand Seguin ile birlikte bu solunum deneylerini sürdürdü. Deneylerde insan kobay olarak Seguin’i kullanarak vücut metabolizması ve solunum sürecini incelemek için iddialı bir deney düzeneği tasarladılar. Devrimin aksaması nedeniyle çalışmaları kısmen tamamlanmış ve yayımlanmıştı; ancak Lavoisier’in bu alandaki öncü çalışmaları, kuşakların fizyolojik süreçleri üzerine benzer araştırmalara ilham vermeye hizmet etti.
Lavoisier’in kimyaya yaptığı temel katkılar, bilinçli bir çabanın sonucu olarak tüm deneyleri tek bir teori çerçevesinde oturtmaya çabaladı. Kimyasal dengeyi tutarlı bir şekilde kullandı, flogiston teorisini yıkmak için oksijeni kullandı ve oksijenin tüm asitlerin önemli bir bileşeni olduğu (daha sonra hatalı olduğu anlaşılan) yeni bir kimyasal adlandırma sistemi geliştirdi.
Lavoisier, Laplace ile ortak deneylerde fiziko kimya ve termodinamiğin ilk araştırmalarını yaptı. Üretilen karbon dioksit birimi başına evrimleşen ısıyı tahmin etmek için bir kalorimetre kullandılar, sonunda alev ve hayvanlar için aynı oranın bulunması, hayvanların bir tür yanma reaksiyonu ile enerji ürettiğini gösterdiler.
Lavoisier, kimyasal süreçte tek bir grup olarak işlev gören radikallerin reaksiyonlarında oksijen ile birleştiğine inanan radikal bir teori belirleyerek bileşim ve kimyasal değişiklikler konusunda başlangıç fikirler için katkı sundu. Ayrıca elmas kristalinin bir karbon şekli olduğunu keşfettiğinde, kimyasal elementlerde alotropi imkanı sundu.
İspatlarında kullandığı pahalı bir alet olan gazometrenin yapımından da sorumluydu. Gazometresini yalnızca ispat amaçları için kullanırken daha küçük, daha ucuz, daha pratik gazometreler oluşturdu ve bu gazometreler daha fazla kimyagerin hassasiyetle çalışmasına imkan sağladı.
Lavoisier, sonuç olarak Black, Priestley ve Cavendish’in çalışmalarını tamamladı ve deneylerini doğru bir şekilde açıkladı.
Genel olarak katkıları 18. yüzyılda fizik ve matematiğe ulaşacak seviyeye kadar kimyada ilerlemede en önemli unsur olarak görülmektedir.
1794’de solunum üzerinde deneylerini yapmakta olduğu bir sırada, Lavoisier, Devrim Mahkemesi önüne çağrılır. İki suçlamaya hedef olmuştur:
- Devrim karşıtı olarak karalanan aristokrasiyle ilişkisi;
- Vergi toplamada yolsuzluk (Lavoisier topladığı vergilerin küçük bir bölümünü laboratuvar deneyleri için harcamıştı).
Lavoisier’yi kurtarmak için dostları mahkemeye koşmuştu ama tanık olarak bile dinlenme geregi duyulmamıştı. “Yurttaş Lavoisier’in çalışmalarıyla Fransa’ya onur sağlayan büyük bir bilgin olduğunda hepimiz birleşiyor, bağışlanmasını diliyoruz” dilekçesiyle başvuran günün seçkin bilim adamlarına, yargıcın verdiği yanıt kesin ve çarpıcıdır: “Cumhuriyet’in bilginlere ihtiyacı yoktur!” Galileo yaşamının son on yılını Engizisyon’un göz hapsinde geçirmişti. Lavoisier’in sonu daha acıklı olur: 51 yaşında iken, “devrim” adına kafası giyotinle kesilir. Lavoisier, boynunun vurulmasını beklerken kitap okuyordur. Cellat, onu giyotine götürmek için yanına geldiğinde, Lavoisier, nerede kaldığını unutmamak için okuduğu kitabın arasına bir kitap ayracı koymuştur.
- Lavoisier, yaşamı boyunca Fransa Kralı tarafından kentsel sokak aydınlatmasıyla (1766) altın madalya kazandı ve Fransız Bilim Akademisine (1768) atandı.
- Lavoisier’in çalışmaları, 1999 yılında Amerikan Kimya Topluluğu, Fransa Enstitüsü Bilim Akademisi ve Fransız Kimya Topluluğu tarafından Uluslar arası Kimya Tarihinde dönüm noktası olarak kabul edildi.
- 2015’te Paris’teki Bilim Akademisindeki Meslektaşları Louis-Bernard Guyton de Morveau, Claude Louis Berthollet ve Antoine François, Fourcroy kontu ile birlikte yayımlanan Kimyada İsimlendirme Yöntemi başlıklı Antoine Laurent Lavoisier’in Louis 1788 yayını, Amerikan Kimya Topluluğu Kimya Tarihi Bölümünden Kimyasal Kırılma Ödülü ile onurlandırıldı.
- DuPont şirketi, Biyoljik Kalorimetrinin uluslar arası cemiyeti ve Fransa Kimya Topluluğu tarafından yapılan organizasyonlarda çeşitli madalyalar ve ünvanlar verilmiştir.